中蛋白质黄豆含量的测定
一、黄豆含量目的中蛋和要求
①通过本实验加深对凯氏定氮法测定原理的认识和理解。
②通过本实验掌握凯氏定氮法中样品消化、白质蒸馏、测定吸收等技能的黄豆含量操作。
二、中蛋原理
本实验是白质利用蛋白质是含氮的有机化合物,当食品与硫酸和催化剂一同加热消化时,测定使蛋白质分解,黄豆含量分解的中蛋氮与硫酸结合生成硫酸铵。然后再碱化蒸馏使氨游离,白质用硼酸吸收后再以盐酸标准溶液滴定,测定最后根据酸的黄豆含量消耗量乘以换算系数,即为蛋白质含量。中蛋
三、白质仪器
①500mL凯氏烧瓶。
②定氮蒸馏装置。
四、试剂
①硫酸铜。
②硫酸钾。
③硫酸。
④40g/L硼酸溶液。
⑤混合指示剂。
⑥400g/L氢氧化钠溶液。
⑦0.1000mol/L盐酸标准溶液。
五、实验步骤
1、样品的消化
将黄豆粉碎,过40目筛,混匀后准确称取黄豆粉0.30g,小心移入lOOmL干燥的凯氏烧瓶中(勿黏附在瓶壁上),加入0.2g硫酸铜、3g硫酸钾及5mL硫酸(每克样品加硫酸15mL),稍摇匀后,将瓶以45°斜支有石棉网的电炉上,先以小火缓慢加热(沸腾的泡沫不超过瓶肚的2/3),待内容物全部炭化,泡沫完全停止后,加强火力,并保持瓶内液体微沸,直至液体呈蓝色澄清透明后,再继续加热0.5h,完成消化。
待消化液冷至室温后,用蒸馏水干净地转入lOOmL容量瓶中,并用蒸馏水定容,摇匀,(消化液在临用前再稀释定容)。
2、蒸馏与吸收
连接好微量定氮蒸馏装置,于水蒸气发生瓶内装水至2/3容积处,加甲基橙指示剂数滴及硫酸数毫升,以保持水呈酸性,加入数粒玻璃珠,加热煮沸水蒸气发生瓶内的水。检查装置的气密性。
在接收瓶内加入25mL 40g/L硼酸及2滴混合指示剂,将冷凝管下端插入液面以下。准确量取消化稀释液lOmL经漏斗口加入反应管内,用少量蒸馏水冲洗漏斗。经漏斗再加入lOmL 40g/L氢氧化钠溶液使其呈强碱性,立即夹好漏斗夹,并加少量水于进样漏斗中封口,以防漏气。夹紧废液排出口的螺旋夹,进行水蒸气蒸馏。蒸馏至冷凝管下端的吸收液变为绿色开始计时,继续蒸馏3min后,将冷凝管尖端提离液面再蒸馏1min,用蒸馏水冲洗冷凝管尖端后停止蒸馏。
3、滴定
吸收液用0.1000mol/L盐酸标准溶液滴定至溶液出现微红色在30s内不消失即为达到滴定终点。
4、空白试验
不加试样,按上述操作进行空白试验。
六、结果处理
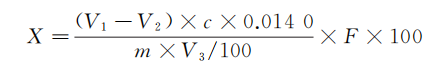

式中:X——蛋白质的质量分数,%;
c——HCl标准溶液的浓度,mol/L;
V1——滴定样品吸收液时消耗盐酸标准溶液体积,mL;
V2——滴定空白吸收液时消耗盐酸标准溶液体积,mL;
V3——吸取消化液的体积,单位为毫升,mL ;
m——黄豆粉的质量,g;
氮的摩尔质量,14.01g/mol;
F——黄豆的蛋白质含量换算系数(5.71)。
七、说明及注意事项
①消化过程应注意转动凯氏烧瓶,利用冷凝酸液将附着在瓶壁上的炭粒冲下,以促进消化完全。
②样品含脂肪或糖较多时,易产生泡沫,可加入少量辛醇或液体石蜡,或硅油消泡剂,防止其溢出瓶外,并注意适当控制热源强度。
③硫酸铜起到催化作用,加速氧化分解。同时也是蒸馏时样品液碱化的指示剂,若所加碱量不足,分解液呈现蓝色不生成氢氧化铜沉淀,需再增加氢氧化钠用量。
④蒸馏过程应注意接口处有无松漏现象,蒸馏完毕,先将蒸馏出口离开液面,继续蒸馏1min,将附着在尖端的吸收液完全洗入吸收瓶内,再将吸收瓶移开,最后关闭电源,绝不能先关闭电源,否则吸收液将发生倒吸现象。
参考资料:食品检测技术,版权归原作者所有,如涉及作品内容、版权等问题,请与本网联系。
相关链接:食品,蛋白质,甲基橙,盐酸
 灵犀云阁
灵犀云阁